저산소 EV와 하이드로젤 결합…차병원, 외상성 뇌손상 병변 40퍼센트 줄였다
저산소 환경에서 생산한 줄기세포 유래 세포외소포체를 생체적합 하이드로젤에 결합해 외상성 뇌손상 병변을 크게 줄이는 기술이 개발됐다. 줄기세포가 아닌 세포외소포체와 전달용 바이오 소재를 결합한 플랫폼으로, 손상 부위에 장기간 치료 신호를 공급해 신경재생과 염증 조절을 동시에 노린 점에서 주목된다. 업계에서는 외상성 뇌손상 치료 패러다임을 바꾸는 비세포 기반 신경재생 전략의 분기점으로 보고 있다.
차의과학대학교 분당차병원은 한인보 신경외과 교수와 이기범 미국 럿거스대학교 교수 공동연구팀이 외상성 뇌손상 치료를 위한 새로운 생체재료 기반 플랫폼을 개발했다고 21일 밝혔다. 연구팀은 저산소 조건에서 배양한 줄기세포 유래 세포외소포체를 생체직교형 하이드로젤인 BIOGEL에 탑재해, 손상된 뇌 부위에 지속적으로 전달하는 방식을 제시했다. 동물 모델에서 병변 크기를 40퍼센트 이상 줄이고 운동 및 인지 기능 회복 효과를 확인했다.
외상성 뇌손상은 사고 직후 발생하는 1차 손상 이후에도 뇌 내부에서 신경염증, 혈관 기능 이상, 신경세포와 지지세포 손실 같은 2차 손상이 연속적으로 진행되는 질환이다. 이 과정은 주변 정상 조직까지 손상시켜 장기적인 운동 기능 저하와 기억·인지 장애를 유발하는 주된 원인으로 꼽힌다. 수술과 약물치료로 출혈과 부종, 염증을 일정 부분 조절할 수 있지만, 이미 손상된 신경 회로 자체를 되살리는 근본 치료는 거의 불가능한 영역으로 남아 있었다.
연구팀은 이러한 한계를 겨냥해 인간 유도만능줄기세포에서 분화시킨 신경전구세포에 저산소 유도제 DFO를 처리해 손상 뇌와 유사한 저산소 환경을 실험실 내에서 구현했다. 그 결과 신경재생과 혈관 신생에 핵심적인 단백질인 VEGF와, 신경발달과 축삭 형성에 관여하는 마이크로RNA miRNA-9가 풍부하게 포함된 세포외소포체를 대량 생산하는 데 성공했다. 세포외소포체는 줄기세포가 분비하는 나노 크기의 소포체로, 손상 조직 회복과 염증 조절 능력이 부각되며 차세대 줄기세포 대체제로 떠오르고 있다.
하지만 세포외소포체를 단독으로 투여할 경우 손상 부위에 충분히 도달하지 못하거나 체내에서 빠르게 소실돼 효과 지속 시간이 짧다는 한계가 지적돼 왔다. 또 반복 투여 시 비용 부담과 제형 안정성 문제도 상용화의 걸림돌로 꼽힌다. 특히 뇌 조직은 구조가 촘촘하고 손상 부위 주변 환경이 불균일해 약물이나 나노입자의 국소 유지가 쉽지 않다.
연구팀은 이러한 전달 문제를 해결하기 위해 젤라틴 기반 생체적합 하이드로젤을 세포외소포체의 운반체로 채택했다. 뇌 조직과 유사한 탄성을 갖도록 설계된 BIOGEL은 손상 부위에 주입되면 주변 조직에 밀착돼 고정된다. 이후 내부에 포집된 세포외소포체를 서서히 방출하면서 손상 영역 전체에 장기간에 걸쳐 치료 신호를 공급한다. 결과적으로 단회 투여에도 지속적인 신경재생과 혈관 재형성을 유도할 수 있는 구조다.
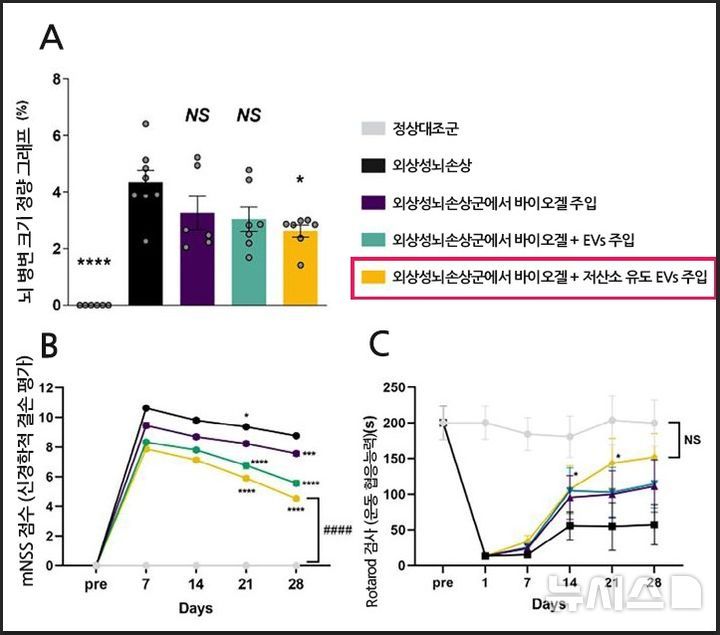
동물 모델 실험에서 연구팀은 외상성 뇌손상 부위에 BIOGEL과 세포외소포체가 결합된 복합체를 주입했다. 그 결과 대조군과 비교해 손상 뇌 조직의 병변 크기가 40퍼센트 이상 감소했다. 조직 수준에서는 신경세포 재생과 축삭 재형성이 촉진됐고, 미세혈관 밀도 증가를 동반한 혈관 재생이 관찰됐다. 염증 관련 지표는 의미 있게 감소했으며, 행동 분석을 통해 운동 기능과 인지 기능의 유의미한 회복도 확인됐다.
한인보 교수는 저산소 조건에서 생산한 세포외소포체의 생물학적 신호를 하이드로젤이라는 물리적 플랫폼에 결합한 점을 핵심 성과로 꼽았다. 그는 저산소 유도 세포외소포체가 갖는 신경보호와 재생 신호를 생체적합 하이드로젤을 통해 안정적이고 장기적으로 전달함으로써, 실제 임상 적용이 가능한 새로운 신경재생 치료 전략의 실마리를 제시했다고 평가했다.
이번 접근법은 기존 세포치료가 가진 면역학적 부담을 줄이면서 치료 효과를 유지하거나 높일 수 있다는 점에서도 주목된다. 살아 있는 줄기세포를 직접 이식하는 방식은 면역 거부 반응과 종양 형성 가능성이 상존해 엄격한 안전성 검증이 필요하다. 반면 세포외소포체는 세포가 아닌 나노 크기의 생체 유래 입자로, 적절한 정제와 품질 관리를 전제로 상대적으로 안전성이 우수하다고 여겨진다. 하이드로젤까지 더해지면 국소 투여로 전신 부작용을 줄이면서도 약리 신호를 집중시킬 수 있다.
연구팀은 이번 플랫폼이 외상성 뇌손상을 넘어 다양한 중추신경계 손상에도 확장 적용될 수 있을 것으로 보고 있다. 척수손상, 허혈성 뇌질환처럼 광범위한 조직 손상과 만성 염증이 동시에 진행되는 질환에서, 저산소 유도 세포외소포체와 하이드로젤 기반 국소 전달 전략이 새로운 옵션이 될 수 있다는 관점이다. 손상 양상과 위치에 따라 하이드로젤의 물성, 분해 속도, 세포외소포체 조성 등을 조정하는 맞춤형 플랫폼으로 진화할 여지도 열려 있다.
한 교수는 줄기세포 유래 생체소재와 나노하이브리드 플랫폼을 활용한 중추신경계 재생 연구를 장기간 수행해 왔으며, 최근에는 생체활성재료, ACS 나노, 생체재료학 등 국제 학술지에 연속으로 연구 성과를 발표했다. 이 같은 연구 성과를 바탕으로 한국을 빛낸 사람들에 11차례 등재되는 등 국내 척추재생 의학 분야를 대표하는 연구자로 평가받고 있다.
이번 연구 결과는 재생의학 분야 전문 학술지 첨단과학회지에 저산소 유도 세포외소포체를 활용한 외상성 뇌손상 치료용 첨단 생체재료 전달 플랫폼을 주제로 게재됐다. 산업계와 의료계에서는 이번 기술이 실제 임상 시험과 규제 검증 과정을 거쳐 외상성 뇌손상 환자의 치료 옵션으로 자리 잡을 수 있을지 주시하고 있다.

