“약물 뇌투과 기술 쟁탈전”…노바티스, 중국 BBB 플랫폼 확보전 가속
퇴행성뇌질환 치료 혁신을 위한 뇌혈관장벽(BBB, Blood-Brain Barrier) 투과 기술 확보 경쟁이 글로벌 제약업계에서 본격화되고 있다. 뇌혈관장벽은 혈액 내 유해물질이 뇌로 유입되는 것을 차단하는 생체 방어선이지만, 동시에 치료제 전달도 막아 퇴행성뇌질환 신약 개발의 난제로 꼽혀왔다. 이에 따라 약물의 뇌 전달을 획기적으로 개선하는 신기술에 전 세계 주요 기업들의 투자가 잇따르고 있다.
중국 바이오벤처 시로낙스는 9일(현지 시간) 노바티스와 'BDM(Brain Delivery Module) 플랫폼'에 대한 독점 옵션 계약을 체결했다고 밝혔다. 이 계약으로 노바티스는 BDM 기술을 우선적으로 인수할 권리를 얻는 한편, 시로낙스는 자체 치료제 개발 권리를 유지한다. 계약 규모는 선급금, 단기 지급금 등을 합해 최대 1억7500만 달러에 이른다. BDM 플랫폼은 약물 분자가 BBB를 효율적으로 통과하는 특수 전달 메커니즘을 기반으로 한다.
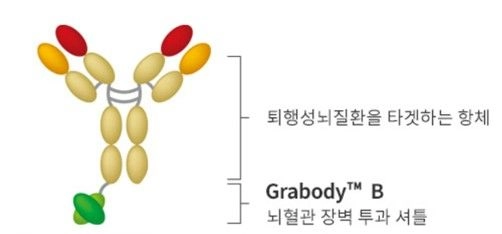
비슷한 시기, 국내 이중항체 전문기업 에이비엘바이오도 GSK와 약 3조9600억원 규모의 뇌 전달 플랫폼 기술이전 계약을 체결했다. 해당 기술 ‘그랩바디-B’는 인슐린 유사 성장 인자1 수용체(IGF1R)를 표적으로 약물을 셔틀하듯 BBB를 투과시킨다. 이 플랫폼 도입으로 기존 약물이 가진 뇌 투과 한계를 근본적으로 개선하며, 퇴행성뇌질환 치료제의 ‘퍼스트 인 클래스’(최초 혁신) 개발이 기대되고 있다.
“특히 이번 기술은 기존 투약 방식이 뇌에 이르지 못하거나, 높은 용량 투여에 따른 전신 부작용 위험을 동반했던 한계를 극복했다.” 업계에서는 뇌질환 치료제 시장이 기술 중심 경쟁구도로 재편될 것으로 보고 있다. 미국 및 유럽 제약사들 역시 다양한 BBB 교차 플랫폼 확보에 투자하는 추세다. 예를 들어 릴리, 자이데나 등도 최근 자체 및 제휴 개발 플랫폼을 확대 중이다.
각국 규제 측면에서도 신약의 BBB 투과성 입증을 임상, 허가 단계에서 엄격히 요구하는 분위기다. 실제 식약처·FDA·EMA 등 허가기관은 안전성과 더불어 뇌 전달 효율·타깃 특이성에 대한 데이터를 중점 심사 기준으로 내세우고 있다. 기술 상용화에 필요한 바이오마커(생체지표) 인증, 장기효과 모니터링, 동물시험과 인체 적용간 차이 검증 등이 핵심 진입장벽이다.
로버트 발로 노바티스 글로벌 신경과학 총괄은 “뇌혈관장벽을 효과적으로 넘는 치료제 전달법은 신약 개발의 결정적 변곡점이 될 것”이라고 평가했다. 산업계는 이번 기술 확보전이 시장 혁신의 단초가 될지 주목하고 있다.
