“두 단백질 협력으로 자외선 손상 DNA 복구”…UNIST, NER 분자 기전 새로 썼다
자외선에 의한 DNA 손상 인식과 복구 과정이 기존 상식을 뒤집는 협력 메커니즘으로 작동함이 UNIST 연구진에 의해 밝혀졌다. 피부노화와 암을 유발하는 손상된 DNA 염기쌍만을 빠르게 찾아내는 복구 경로를 분자 차원에서 규명한 이번 연구는, 병변 신속 탐지 효율이 전체 복구 과정을 좌우한다는 점에서 산업적 파급력도 주목된다. 업계와 학계는 이번 결과를 “DNA 복구 경쟁의 게임체인저”로 평가하고 있다.
3일 울산과학기술원 생명과학과 이자일 교수팀은 ‘NER(핵산 절제 복구, Nucleotide Excision Repair)’ 경로에서 핵심적으로 작용하는 XPC와 UV-DDB 두 단백질이, 기존의 일대일 순차 협력이 아닌 복합체(UX-complex)로 결합해 손상 부위를 탐색·복구한다는 것을 규명했다고 발표했다. 이들 단백질의 작용 방식은 세계적 학술지 ‘뉴클레익 에시드 리서치’ 6월 18일 온라인 판에 게재됐다.
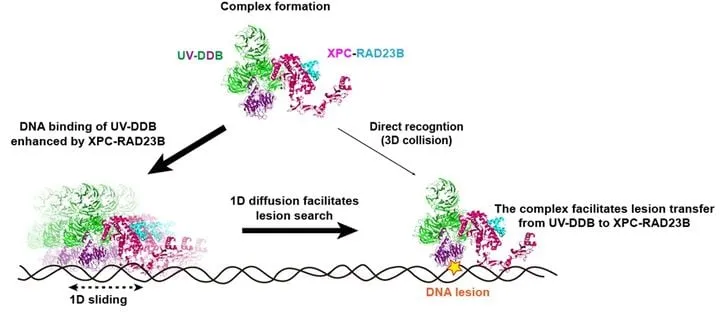
분자생물학적으로 NER은 자외선에 의해 생긴 CPD(싸이클로부탄 피리미딘 다이머) 등 손상 구조를 DNA에서 정밀히 잘라내 복구하는 경로다. DNA 속 30억 개 염기쌍 중 손상 위치를 빠르고 정확히 탐지하는 일이 효율의 관건이다. 그간 XPC 단백질이 구조 변화를 감지해 손상 부위를 표시하는 역할을 맡는 것으로 알려졌으나, CPD와 같은 미세 손상의 경우 XPC 단독 인식이 어렵다는 한계가 제기돼 왔다.
이번 연구에서 주목할 부분은 UV-DDB 단백질이 탐지력 보조자 역할을 넘어서 XPC와 복합체(UX-complex)를 형성하며 “동적 협력” 구조를 띤다는 점이다. UX-complex 상태에서는 UV-DDB가 손상 DNA 가닥에 더 강하게 결합하는 동시에, DNA 가닥을 따라 미끄러지듯 이동하면서 손상 탐색 능력이 대폭 향상된 것으로 분석된다. XPC와 UV-DDB의 상호작용이 단백질-유전자 복구 경로를 효율적으로 촉진한다는 점에서, 기존 분자생물학 교과 내용까지 수정될 가능성도 제기된다.
시장 및 질환별 활용 측면에선, UX-complex의 협동적 작동 기전을 표적으로 한 DNA 복구 촉진제 개발이나 피부암·노화 예방 신소재 분야 등 산업 수요 확장성도 거론된다. 특히 색소건피증(Xeroderma Pigmentosum)과 같이 XPC 유전자 결함으로 피부암 위험이 극단적으로 커지는 질환에서, 복구 기전의 세밀한 조절은 환자 맞춤형 치료전략 근거가 될 수 있다.
전 세계적으로도 NER 핵심 단백질의 협력 원리에 대한 규명은 드문 사례로, 미국, 일본 등 선진국 의생명연구 현장에서도 후속 파급 효과가 예상된다. 최근 미국의 NIH나 유럽의 분자진단 업체들이 DNA 손상·복구 플랫폼 고도화에 경쟁적으로 투자 중이라는 점도 주목된다.
한편, DNA 복구의 임상적용을 위한 Next-Gen 플랫폼 개발이나 데이터 신뢰성, 인체적용 윤리 등 규제 이슈 역시 산업화의 필수조건으로 부상하고 있다. 국내외적으로 항노화·암예방 분야 ICT·바이오 융합 제품 시장 진입도 규제 및 기술 고도화와 병행이 요구된다.
이자일 교수는 “이번 연구는 자외선에 의한 DNA 손상 탐지·복구의 패러다임을 협력적 복합체 관점에서 재해석한 것으로, 향후 피부암·노화 대응 바이오 신산업에 전략적 전환점을 제시할 수 있다”고 강조했다. 산업계는 이번 과학적 진전이 실질적으로 시장 혁신으로 이어질지 예의주시하고 있다.
