“코그테라, 디지털치료제 시대 본격화”…식약처, 의료기기 허가 확대→치료 패러다임 변화
디지털치료제 분야가 변화의 바람을 맞이하고 있다. 식품의약품안전처는 5월 한 달 동안 의료제품 123개 품목을 허가하며 혁신 흐름을 가속화했다고 11일 밝혔다. 최초로 경도인지장애 환자의 인지기능 저하를 늦추는 디지털의료기기 ‘코그테라(Cogthera)’가 국내 시장에 발을 들이며, 디지털 기반 신치료 패러다임의 서막을 연 것이다.
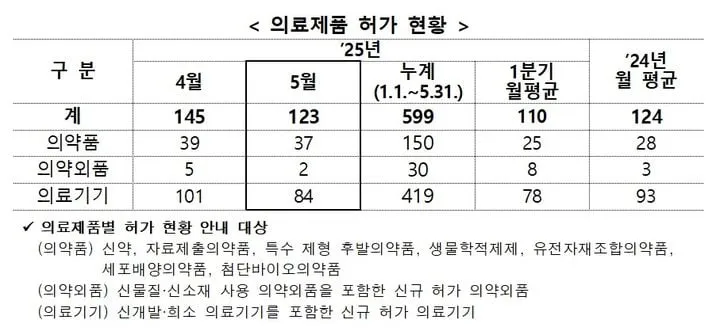
식품의약품안전처에 따르면, 5월 허가된 품목은 의약품 37개, 의료기기 84개, 의약외품 2개로 분류된다. 지난해 월평균(124개)에 근접하는 수준이고, 올해 1분기 평균(110개)보다 11.8% 증가해 국내 의료제품 시장의 활력이 뚜렷하게 나타났다. 희귀의약품 부문에서는 간질성폐질환 치료 신약 ‘오페닙정’과 소세포폐암 3차 치료제 ‘임델트라주’가 허가를 받으며 희귀·난치질환 환자 치료의 지평을 넓혔다. 특히 주목할 점은 디지털의료기기 부문에서, 코그테라가 경도인지장애 환자의 인지기능 악화 지연을 목표로 한 인지 치료 소프트웨어로 국내 첫 승인 사례가 됐다는 사실이다. 인공지능과 디지털 헬스케어 기술의 융합으로, 기존 약물 치료에 비해 부작용이 적고 맞춤형 케어가 가능하다는 평가를 받고 있다.
식약처는 “안전성과 유효성이 검증된 혁신 의료기기의 신속 허가를 통해 환자의 치료 접근성을 넓히는 한편, 투명한 허가 심사로 제품 신뢰도를 높이겠다는 방침”이라고 밝혔다. 다가올 고령사회와 인지장애 환자 증가에 대응해, 디지털의료기기의 빠른 도입은 의료 현장의 치료 옵션을 실질적으로 확장시키고 있다. 전문가들은 국내 시장에서의 디지털치료제 상용화가 향후 의료 패러다임을 근본적으로 전환할 가능성을 높게 평가하며, 안전성과 임상적 효과를 확인한 후속 제품 개발도 가속할 것으로 내다봤다.
