“돼지 심장판막 인간화”…서울대병원, 이종조직 재세포화 첫 성공
이종조직의 면역 거부항원을 제거하고 인간 세포를 정착시킨 심장판막 개발이 본격화되고 있다. 서울대학교병원 연구팀이 동물 심장판막 조직에서 인체 면역 반응의 원인인 ‘이종항원’을 제거하고, 여기에 사람 세포를 공배양해 체외에서 조직 생존과 재생을 유도하는 데 성공했다. 바이오업계는 해당 기술이 반복적 심장판막 수술의 한계를 넘어서는 ‘이종조직 기반 치료’ 경쟁의 분기점으로 평가하고 있다.
서울대병원 김소영 연구교수, 김기범 소아청소년과 교수, 임홍국 소아흉부외과 교수 팀은 돼지에서 유래한 심장판막 조직을 ▲α-Gal, ▲Neu5Gc 등 면역 거부항원 제거와 ▲인간 중간엽 줄기세포 및 내피세포 이식 등 이중 전략으로 처리했다. 13일 발표된 이번 연구는 탈세포화(Decellularization)와 두 가지 효소(α-갈락토시다아제, PNGase-F) 동시 처리로 항원(immune antigen) 소거 효과를 극대화하고, 실제 인간 세포의 고착 및 조직화 가능성까지 입증한 것이 핵심이다.
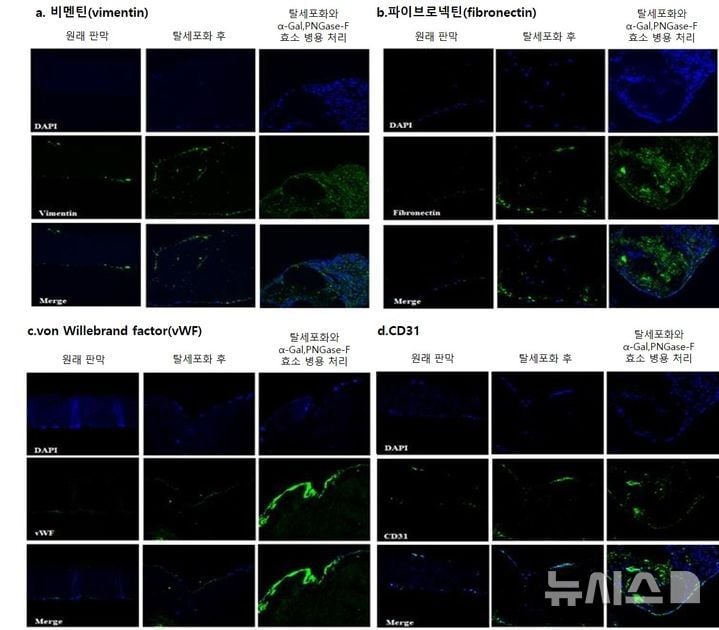
이 과정에서 ‘삼중 시너지 효과’가 관찰됐다. 첫째, 조직의 생체역학적 안정성(구조와 강도)을 유지하며, 둘째, 주요 면역항원을 제거했으며, 셋째, 탄수화물 결합 렉틴 신호까지 줄였다. 두 종류의 인간 유래 세포(지방 줄기세포, 제대정맥 내피세포)를 공배양했을 때 비멘틴, 칼포닌, 파이브로넥틴, von Willebrand factor 등 재세포화 지표 단백질 발현도 현저히 증가했다. 이는 조직이 살아 있는 것처럼 미세환경을 재구성했음을 보여준다.
실제 이종조직판막은 돼지·소의 심장 판막 조직을 최대한 가공한 뒤 심장수술 이식재로 널리 활용되지만, 잔존 항원이 인체에서 강한 면역 거부 반응을 일으키고, 특히 소아 환자에서는 성장에 따라 판막 교체가 반복될 수밖에 없는 난제가 있다. 이번 기술은 두 가지 항원을 동시에 제거해 거부반응 억제율을 높이고, 인간 세포가 판막에 직접 자리 잡을 수 있게 해 조직의 재생 및 기능적 수명을 확장한 것이 특징이다. 특히 기존 탈세포화 조직과 단순 효소처리 조직 대비, 안정된 구조와 재생 유도 효과 모두 월등히 개선됐다.
경쟁기술 측면에서 미국·유럽 등에서는 부분 항원 제거 또는 단일 세포 이식 연구가 일부 진행 중이나, 두 항원을 동시 제거하고 환자 세포와의 공배양으로 재생 가능성을 실제 입증한 사례는 거의 전무하다. 학계는 이를 “이종조직 심장판막 이식의 새로운 글로벌 기준”으로 주목하고 있다.
제도적으로는 동물 조직 이식재는 현재 식약처, 미국 FDA 등에서 안전성과 면역 거부 발생률을 엄격히 관리한다. 항원 제거·재세포화 기반 기술의 경우, 전임상(동물) 및 임상 단계를 통한 추가 입증이 요구된다. 동시에, 줄기세포 활용·유전체 변형 여부에 대한 생명윤리 검증 절차도 강화될 전망이다.
임홍국 교수는 “탈세포화와 두 효소 병용처리, 세포 공배양 단계를 결합해 환자 맞춤형 이종조직 재생 가능성이 열린 만큼, 실질적 환자 치료로 연결될 수 있도록 후속 연구를 이어갈 계획”이라고 말했다.
서울대병원은 앞서 자체 항석회화 프로토콜을 적용한 폐동맥 스텐트 판막을 개발해 872명의 환자에게 우수한 임상 결과를 얻기도 했다. 산업계는 이번 심장판막 재세포화 기술이 실제 임상까지 이어질지를 예의주시하고 있다.

