“AI가 항체 결합 구조까지 설계”…갤럭스, 8개 타깃 신약 후보 확대
인공지능 기반 단백질 설계 기술이 신약개발의 혁신 흐름을 주도하고 있다. 갤럭스가 발표한 단백질 설계 플랫폼 ‘갤럭스 디자인’ 성과는 이 기술이 실제로 다양한 질환 타깃에 적용될 수 있음을 보여준다. 특히 알려진 항원-항체 구조 정보가 없는 타깃에 대해서도 완전히 새로운(드노보) 항체를 설계, 정밀 치료제 개발의 패러다임이 현실화 단계에 접어들었다는 분석이다. 업계는 이번 공개가 ‘AI 신약개발 플랫폼 경쟁’의 확실한 분기점이 될 수 있다고 본다.
갤럭스는 최근 PD-L1, HER2, EGFR(S468R), ACVR2A/B, FZD7, ALK7, CD98hc, IL-11 등 8개 단백질 타깃에 대한 항체 설계 성공 사례를 내놨다. 이 중 항노화 타깃인 IL-11과 뇌질환 치료 타깃인 CD98hc에 대한 설계 성과는, 3월 발표한 6개 타깃에 더해 플랫폼의 확장성을 직접 검증했다는 점에 의미가 있다. IL-11은 기존에 알려진 항원-항체 결합 구조 정보가 없던 타깃으로, 갤럭스는 다양한 결합 부위에 작용하는 항체까지 설계하며 신약 후보의 기능적 다양성도 확보했다.
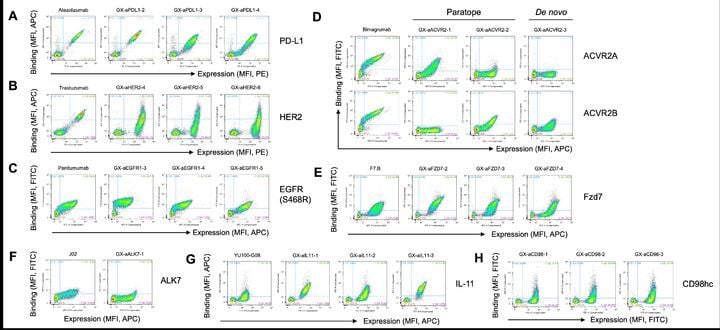
기술적으로 가장 주목되는 부분은 PD-L1 항체의 구조 검증이다. 갤럭스는 극저온 전자현미경(Cryo-EM) 기법을 통해 AI가 설계한 항체와 PD-L1 단백질 간 결합 구조를 원자 수준에서 분석했다. 결과적으로 실험에서 확인된 구조가 AI가 예측한 모델과 거의 완전히 일치해, AI 설계 기반 항체의 정밀성을 입증했다. 특히 이 항체는 기존에 보고된 PD-L1 항체와 다른 결합 방식을 보여, 새롭게 설계된 약물의 독창성까지 확인됐다.
이러한 AI 기반 항체 설계는 신약개발 프로세스 전반의 효율성 향상에 기여하는 것으로 평가된다. 신약 후보 물질을 직접 설계함으로써 효능이 높고 부작용이 적은 약물 도출이 가능해지고, 개발 초기 단계에서 실패 확률을 크게 줄일 수 있다. 해외 바이오테크 업계에서도 인실리코 메디신, 리커전 등 AI·단백질 구조 예측 기술을 적용한 신약개발 경쟁이 이어지는 상황이다.
신약 분야에서 AI 설계 항체의 승인은 아직 초기 단계이지만, 미국 FDA와 유럽 EMA 등도 AI 사용 신약개발의 임상 적용에 대한 가이드라인 정비에 나서고 있다. 국내에서도 식품의약품안전처가 AI 융합 신약과 관련된 사전 심사체계 마련을 준비하면서, 한층 치열한 플랫폼 경쟁 환경으로 접어든 모습이다.
석차옥 갤럭스 대표는 “정밀 치료제 설계로 신약개발의 성공률을 높이는 것은 물론, 약물 설계 자체가 목적과 기능에 맞춰 이뤄지는 시대가 시작됐다”고 밝혔다.
산업계는 이번 AI 항체 설계 기술이 실제 파이프라인 상용화로 이어질 수 있을지 주목하고 있다.

